INTRODUCCIÓN
Las crisis epilépticas (CE) comprenden aproximadamente el 1 % de las consultas en las áreas de Urgencias31. Las diferentes situaciones urgentes relacionadas con crisis epilépticas comprenden:
Crisis sintomáticas agudas (CSA)
Las CSA son aquellas que suceden como consecuencia directa o en estrecha relación temporal con un factor precipitante: metabólico, tóxico, estructural, infeccioso o inflamatorio, que causa una afectación aguda cerebral, pero que no conllevan un diagnóstico de epilepsia. Las CSA no precisan tratamiento anticrisis a largo plazo, aunque en ocasiones puede ser necesario un tratamiento hasta que la situación aguda se resuelva.
Teniendo en cuenta las distintas etiologías32:
- Traumatismo cráneo-encefálico (TCE), incluyendo hematomas epi/subdurales y cirugías intracraneales. Dentro de la primera semana en caso de TCE, pero en casos de hematomas subdurales/cirugías, se aceptan intervalos más prolongados de un mes. En cuanto al tratamiento, hay estudios que demuestran una eficacia similar de FAC clásicos, concretamente fenitoína (PHT) como de nuevos FAC como levetiracetam (LEV), o lacosamida (LCM)33.
- Ictus (isquémico/hemorrágico). Dentro de la primera semana. En las últimas recomendaciones no está justificado el inicio de medicación anticrisis tras una CSA postictus, sin preferencia por ningún FAC. Si se inicia, no está justificado mantenerla más de 7 días34.
- Infección neuromeníngea (meningoencefalitis): durante el curso de la infección. Evitar fármacos que tengan interacciones con el tratamiento de la infección.
- Neurocisticercosis: durante el estadio vesicular-granular (presencia de parásitos), o en la fase transicional/degenerativa. La presencia de granulomas calcificados no se considera CSA.
- Malaria. Las crisis en la fase de fiebre y parasitemia se consideran CSA.
- Abscesos y tuberculomas. En la fase aguda y durante el tratamiento, se consideran CSA. Tras el tratamiento eficaz, no se consideran CSA. Evitar FAC con interacciones con los tratamientos.
- Infección por VIH. En caso de infección aguda o por alteraciones metabólica graves se considera CSA. En caso contrario y sin infecciones oportunistas no se considera como tal.
- Tóxicos/abstinencia (benzodiacepinas, alcohol). En el momento más Los tóxicos con riesgo más elevado son cocaína, anfetaminas, éxtasis, crack. En caso de las crisis en contexto de abstinencia, están indicadas las benzodiacepinas.
- Metabólico, durante la fase de descompensación. Los niveles propuestos para considerar CSA serían: glucosa < 36 o > 450 mg/dl; sodio < 115 mg/dl; calcio < 5 mg/dl; magnesio < 0,8 mg/dl; creatinina > 10 mg/dl.
- Crisis febriles en edad pediátrica (Tª > 38º y sin infección meníngea).
- Esclerosis múltiple. Si ocurre en los primeros 7 días en un
- Enfermedades sistémicas (autoinmunes). En los brotes o fase activa se consideran
Primera CE no provocada
En el caso de una primera CE no provocada se ha de considerar tratamiento cuando exista un riesgo importante de recurrencia. Teniendo en cuenta la última definición de epilepsia propuesta por la ILAE35, se trata de una alteración cerebral en la que:
- Existen más de dos CE no provocadas en un tiempo entre ellas > 24 horas.
- Una sola crisis pero una probabilidad de recurrencia de más del 60 % a los 10 años.
- Existe un síndrome epiléptico definido.
Esta nueva definición nos obliga ante una primera CE a llegar a establecer este riesgo lo más precozmente posible para realizar un diagnóstico y plantear tratamiento.
Consideraciones a tener en cuenta una vez descartadas causas sintomáticas agudas (metabólicas, tóxicas, infecciosas, traumática o vascular aguda):
- Historia clínica exhaustiva
- Episodios previos. Con frecuencia una supuesta primera CE en urgencias no es en realidad una primera crisis. Se ha de incidir ante cualquier síntoma previo que sugiera crisis: convulsión, pérdida de conocimiento, incontinencia o mordedura nocturna, alteración del nivel de conciencia, mioclonías, síntomas sugestivos de auras…
El riesgo de una primera CE generalizada no provocada se sitúa entre el 34-56 % a los 5 años36. Sin embargo, cuando se trata de una segunda crisis este riesgo aumenta al 73 % a los 5 años.
- Antecedentes específicos. Tener en cuenta antecedentes como retraso intelectual, meningitis o convulsiones febriles en la infancia, que pueden orientar hacia un síndrome epiléptico determinado.
Preguntar por comorbilidad que pueda aumentar el riesgo de presentar crisis epilépticas haciendo hincapié en la comorbilidad psiquiátrica.
- Horario de las crisis. La presencia de crisis durante el sueño parece aumentar la probabilidad de recurrencia en los primeros 4 años.
- Lesión en neuroimagen: TC/RM
La presencia de diferentes lesiones crónicas o progresivas en las pruebas de neuroimagen aumenta el riesgo de recurrencia.
Un patrón de imagen de TC anormal aumenta el riesgo; no obstante, mucha de la patología sólo puede ser evaluada por RM craneal, por lo que esta exploración debería completarse en caso de que la TC no demuestre cualquiera de las siguientes patologías: gliosis, encefalomalacia, neoplasias, lesión vascular parenquimatosa crónica cortical/territorial, malformación arteriovenosa/cavernomas, anomalías del desarrollo cortical, anomalía del hipocampo-esclerosis mesial temporal, agrandamiento de los ventrículos > 1,5 cm, o prominencia de espacios de LCR extraxiales > 1,0 cm.
Indicaciones: todo paciente con primera CE ha de realizarse una TC en Urgencias. Ha de completarse con RM craneal en las primeras 72 horas si la TC no es concluyente.
- Hallazgos en el EEG
La presencia de alteraciones epileptiformes en el EEG se relaciona con una alta probabilidad de recurrencia, entre 64-77 %, tanto en población pediátrica como adulta37. No obstante, una de las limitaciones del EEG es la baja sensibilidad para el diagnóstico de crisis, y la prevalencia de anormalidades epileptiformes de crisis de nuevo inicio varía entre 12 y 56 %; no obstante, parece que la rentabilidad diagnóstica del EEG aumenta cuando se realiza de manera precoz tras la primera CE. Los periodos precoces recogidos en estas publicaciones son arbitrarios y variables; no obstante, algunos estudios recomiendan la realización de EEG en las primeras 24 horas.
Indicación: todo paciente con primera crisis ha de realizarse un EEG en las primeras 12-24 horas.
CRISIS URGENTE
Concepto de crisis urgente
Una crisis urgente es aquella que requiere de una atención prioritaria. En este concepto se incluye el estado epiléptico (EE), crisis repetidas en acúmulos y crisis de alto riesgo de evolucionar a un estado epiléptico, teniendo en cuenta puntuación en escalas como la escala ADAN38 o comorbilidad o circunstancias asociadas que aumenten el riesgo de recurrencia de crisis.
Estado epiléptico y crisis potencialmente graves
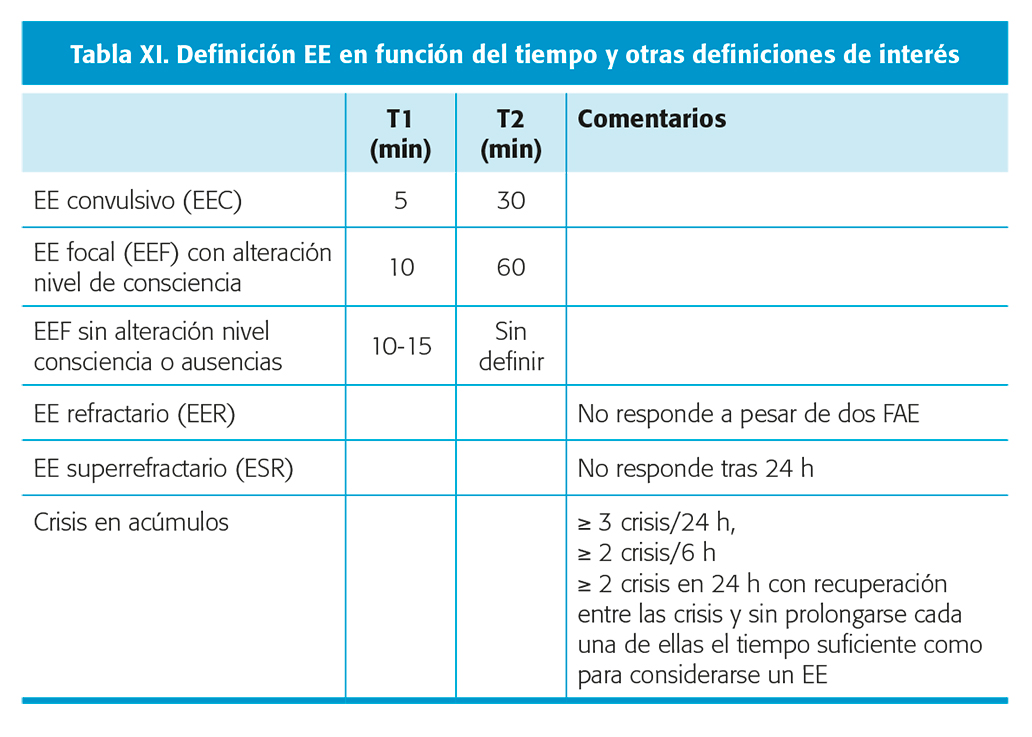
El estado epiléptico (EE) es una emergencia neurológica que representa aproximadamente el 10 % de crisis urgentes y se asocia una mortalidad del 20 % a corto plazo. En 2015, el grupo de trabajo de la Liga Internacional contra la Epilepsia (ILAE) propuso una nueva definición de EE y definió claramente tiempos de actuación t1 y t2: en un EE fallan los mecanismos de terminación de crisis o los de inicio de la misma provocando una duración excesiva (t1), lo cual genera alteraciones estructurales y puede causar déficits irreversibles (t2)39 (tabla XI).
Otras situaciones que suponen un mayor riesgo asociado a las crisis y, por tanto, un cuidado especial y atención urgente son la coexistencia de comorbilidad psiquiátrica, mala adherencia terapéutica, y situaciones especiales como la gestación, cuadro febril asociado, trauma craneal o u otras lesiones asociadas a las crisis como quemaduras.
Tratamiento urgente de las crisis
En la atención urgente la familia y cuidadores, así como los servicios de emergencias extrahospitalarios (SEEH) tienen un papel clave para la administración precoz de medicación, y es importante que existan protocolos claros de actuación que agilicen y faciliten el manejo terapéutico.
- FASE PRE-HOSPITAL (las recomendaciones se basan en opiniones de expertos y las guías sobre tratamiento de EE).
I.A.1 Medidas generales
Las personas cercanas al paciente deben recibir formación para:
- Proteger vía aérea en caso de crisis que curse con alteración del nivel de consciencia (postura de seguridad, no introducir ningún objeto en la cavidad oral en el momento de la crisis, vigilar cavidad bucal cuando ceda la crisis, control de vómitos).
- Retirar cualquier objeto con el que pueda golpearse.
- Intentar describir la semiología de la crisis para facilitar la identificación de la misma y, en la medida de lo posible, cronometrar el tiempo.
Personal sanitario:
- Preservación de la vía aérea: es importante tener en cuenta que la hipoventilación y descenso en saturación de oxígeno tras una crisis suele recuperarse espontáneamente o con aporte de O2 (al 30 % manteniendo una saturación nunca
< 85 %) sin ser preciso la intubación orotraqueal (IOT).
- Asegurar acceso venoso (vía periférica).
- Medida de glucemia y administración de sueroterapia con glucosa, tiamina y
- Retirar objetos o ropa que pueda dañar al paciente y asegurar postura de
- Es importante también anotar tiempos de actuación y de las crisis, así como registrar datos semiológicos y asegurar toma del tratamiento
I.A.2. Tratamiento farmacológico
Todos los estudios publicados recientemente concluyen que la administración precoz de BZD es fundamental para el pronóstico de la persona que sufre una CE40. Para conseguir una administración muy precoz, es fundamental la formación de los pacientes, y cuidadores. En la fase prehospitalaria y en el contexto del domicilio se prioriza la utilización de FAC por vía oral/nasal fácilmente administrables y con acción inmediata41. Las BZD disponibles para administración rápida por vía no intravenosa (IV) son MDZ nasal, oral e intramuscular (IM), LRZ oral y DZP rectal. De éstos, el DZP rectal y el MDZ IM están aprobados mientras que el MDZ nasal, bucal u oral, LRZ oral o DZP oral se pueden utilizar, pero fuera de indicación. Estudios recientes demuestran la superioridad de MDZ sobre DZP rectal tanto por vía oral como nasal como IM42. No se ha comparado hasta el momento LRZ oral con otras BZD. Por vía IV el DZP y LRZ han demostrado una eficacia similar43 y recientemente se ha demostrado la superioridad de CNZ sobre el LRZ IV, teniendo mejor perfil de efectos adversos (EA)44.
Si consideramos FAC de segunda línea, como ya hemos comentado en estos momentos, se lleva a cabo un estudio comparando PPHT, VPA y LEV en EE refractarios a dosis adecuadas de BZD45, sin resultados preliminares hasta el momento.
En crisis prolongadas, que según los tiempos referidos previamente cumplan criterios de EE, se recomienda una biterapia precoz (en los primeros 20 minutos)46: BZD más uno de los FAC de segunda línea disponibles en el momento actual. Aunque no hay estudios que demuestren mayor eficacia de uno sobre otro, sí que hay estudios de no inferioridad que indican efecto similar entre los diferentes FAC. Considerando aspectos de seguridad, un informe reciente del Ministerio de Empleo y Seguridad Laboral Social, ha incluido a la PHT y VPA como fármacos de riesgo para el personal laboral indicando medidas especiales para su administración que pueden retrasar la misma con las implicaciones que esto tiene en el ámbito de la urgencia.
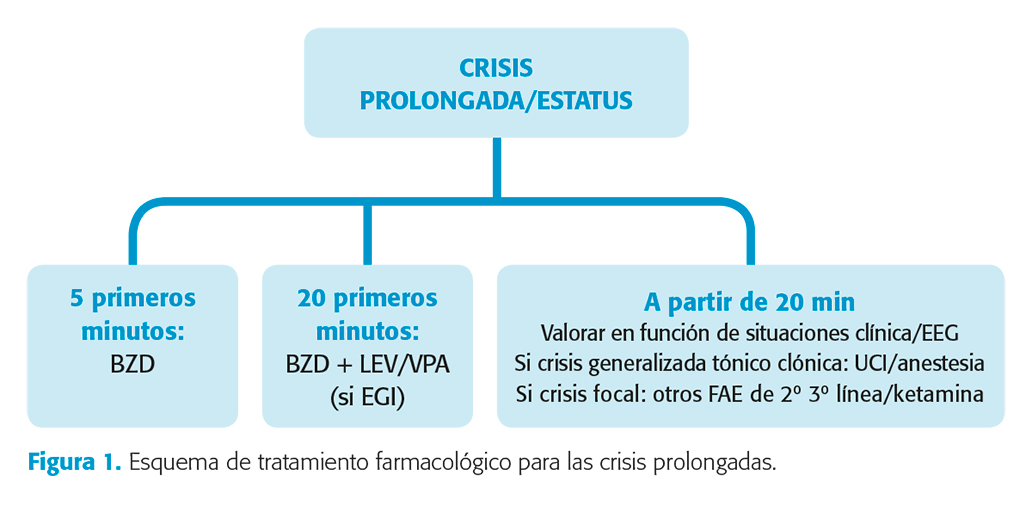
Siguiendo las guías publicadas en la literatura y opiniones de expertos y teniendo en cuenta lo dicho en cuanto eficacia y seguridad, proponemos el siguiente esquema de tratamiento (fig. 1).
- FASE HOSPITALARIA. Consideramos que un paciente con crisis debe ser valorado de forma precoz por neurología, y en función de la clínica decidir pruebas a realizar y tratamiento.
I.B.1. Si el paciente se encuentra en su situación basal
Es prioritario conocer cómo sigue el tratamiento habitual y si lo ha tomado en ese día, ya que la causa más frecuente de aumento en frecuencia de crisis en pacientes con epilepsia es una mala adherencia terapéutica. En caso de que no lo haya tomado o haya dudas, se debe administrar en la urgencia lo más precozmente posible.
I.B.2. Si no se ha recuperado totalmente
Es prioritario descartar que esté teniendo crisis sutiles o bien estatus no convulsivo, por lo que es fundamental realizar un EEG de forma precoz. Además, debemos descartar otras posibilidades como infecciones o alteraciones metabólicas mediante un análisis de sangre.
Si el paciente continúa con crisis:
- Crisis parciales recurrentes o estatus no convulsivo: iniciar tratamiento farmacológico precozmente, biterapia en los primeros 20 minutos, en la fase hospitalaria estaremos ya en este tiempo o lo habremos superado; por tanto, es fundamental asegurar un tratamiento en biterapia a las dosis adecuadas:
- Si no ha recibido BZD: administrar BZD según pauta (tabla XII para dosis).
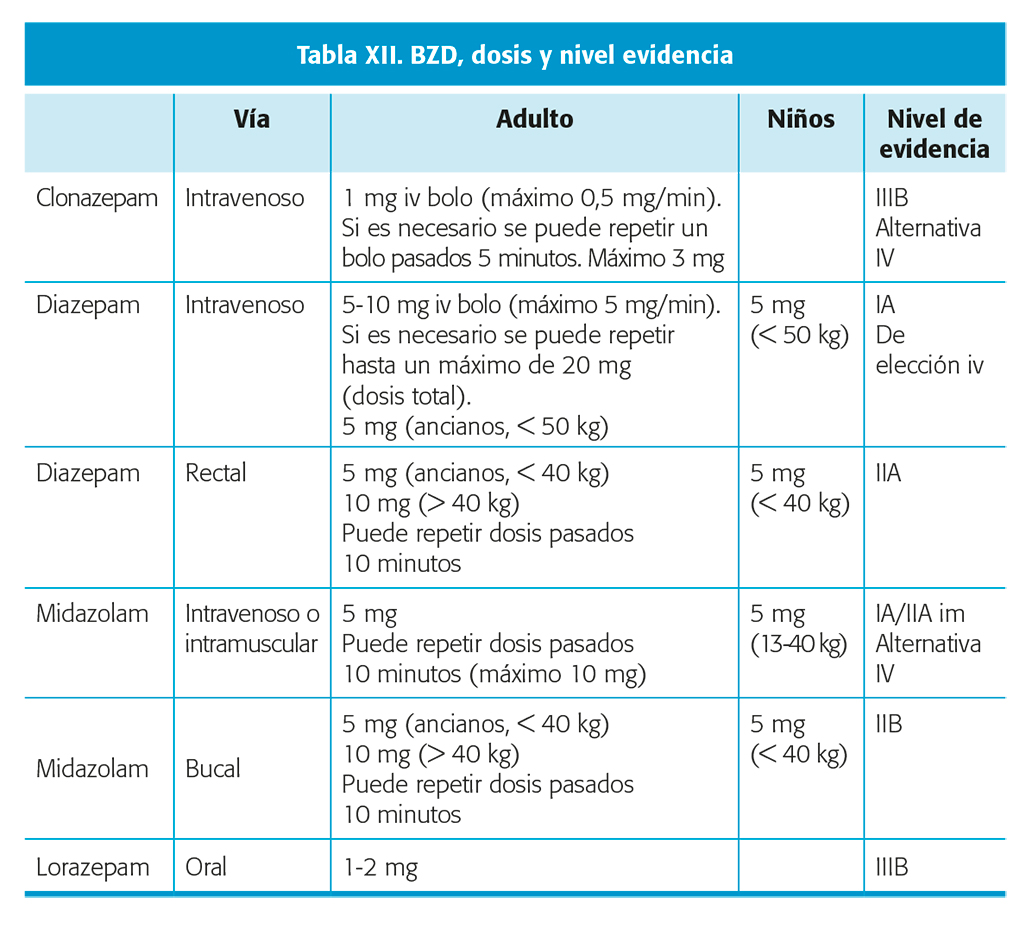
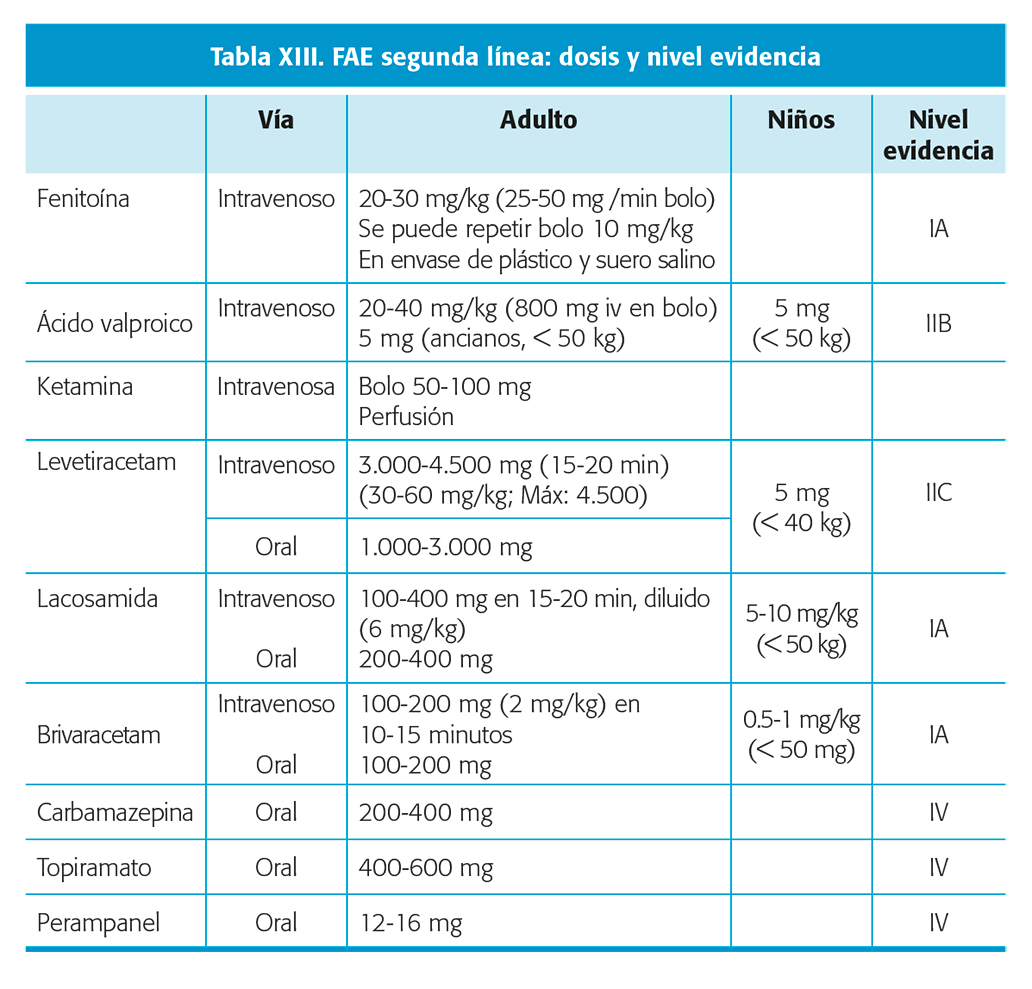
- Si ya ha recibido BZD en dosis adecuada: FAC segunda línea (tabla XIII), considerando en este caso (estatus no convulsivo/crisis parciales recurrentes) también la LCM atendiendo a estudios publicados, al resultado del ensayo reciente (TRENDS) y a las recomendaciones de guías internacionales47.
- Si el paciente no ha tomado adecuadamente su medicación habitual, administrarla vía endovenosa en dosis de carga (si hay disponibilidad endovenosa).
- En cualquier caso, asegurar que se administra adecuadamente medicación habitual. Contactar con Unidad de Cuidados Intensivos (UCI) para valorar traslado si las crisis no ceden (sobre los 60 minutos si hay alteración del nivel de conciencia) y/o cuando exista compromiso hemodinámico.
- Crisis generalizada tónico clónica: valorar inicio de coma anestésico (contactar con UCI) o uso de ketamina (priorizar ketamina, según las dosis (tabla XIV)48.
Mantener tratamiento con los FAC utilizados previamente. Controlar la respuesta con vEEG. Traslado a UCI.
En caso de pacientes sin epilepsia conocida que acuden por crisis, hacer estudio etiológico en el hospital y valorar siempre la patología autoinmune y, en caso de EER o EESR sin causa, iniciar tratamiento con inmunoterapia (corticoides).

CAMBIOS CLÍNICOS EN PACIENTES CON EPILEPSIA CONOCIDA
Las causas de consulta urgente en pacientes con epilepsia conocida son el aumento en la frecuencia de crisis, crisis de mayor intensidad (ya comentados) o bien efectos adversos de la medicación49.
En cualquier caso, es importante siempre realizar una anamnesis completa que nos permita conocer la situación clínica del paciente y los posibles factores desencadenantes de sus síntomas.
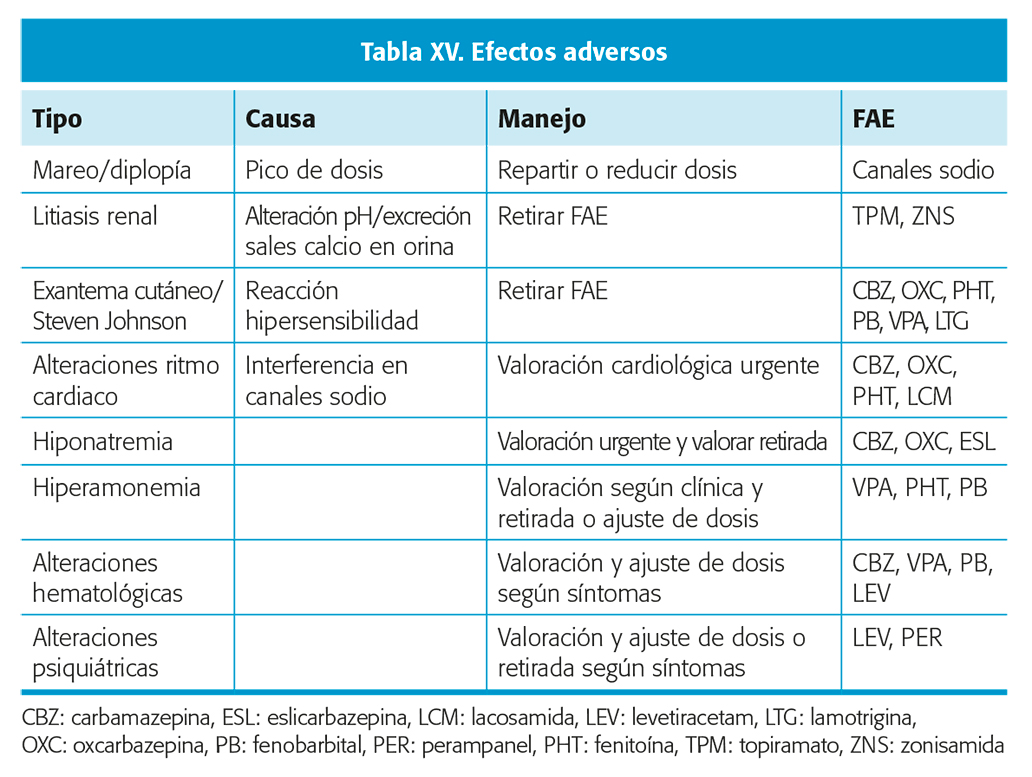
EFECTOS ADVERSOS
Aunque la mayoría de los efectos adversos (EA) tienen curso crónico e instauración subaguda, algunos FAC asocian EA que pueden tener curso agudo y ser invalidantes (tabla XV). Es importante valorar los síntomas que aparecen tras el inicio del tratamiento.

Bibliografía
- Mercadé Cerdá JM, Toledo Argani M, Mauri Llerda JA, López Gonzalez FJ, Salas Puig X, Sancho Rieger J. The Spanish Neurological Society official clinical practice guidelines in Neurologia 2016;31(2):121–9.
- Beghi E, Carpio A, Forsgren L, Hesdorffer DC, Malmgren K, Sander JW, et Recommendation for a definition of acute symptomatic seizure. Epilepsia. 2010; 51(4): 671–5.
- Kwon SJ, Barletta JF, Hall ST, Mangram AJ, Dzandu JK, Abdulhamid M, et al. Lacosamide versus phenytoin for the prevention of early post traumatic J Crit Care. 2019; 50: 50-3.
- Holtkamp M, Beghi E, Benninger F, Kälviäinen R, Rocamora R, Christensen H; European Stroke Organisation. European Stroke Organisation guidelines for the management of post-stroke seizures and Eur Stroke J. 2017. 19; 2 (2): 103-15.
- Fisher RS, Acevedo C, Arzimanoglou A, Bogacz A, Cross JH, Elger CE, et ILAE official report: a practical clinical definition of epilepsy. Epilepsia. 2014; 55(4): 465-82.
- Krumholz A, Wiebe S, Gronseth GS, Gloss DS, Sanchez AM, Kabir AA, et Evidence-based guideline: management of an unprovoked first seizure in adults: Report of the Guideline Development Subcommittee of the American Academy of Neurology and the American Epilepsy Society. Neurology. 2015; 84(16): 1705-13.
- Bouma HK, Labos C, Gore GC, Wolfson C, Keezer MR. The diagnostic accuracy of routine electroencephalography after a first unprovoked seizure. Eur J Neurol. 2016; 23 (3):455-63.
- Requena M, Fonseca E, Olivé M, Abraira L, Quintana M, Mazuela G, et The ADAN scale: a proposed scale for pre-hospital use to identify status epilepticus. Eur J Neurol. 2019; 26(5): 760-e55.
- Trinka E, Cock H, Hesdorffer D, Rossetti AO, Scheffer IE, Shinnar S, et al. A definition and classification of status epilepticus-Report of the ILAE Task Force on Classification of Status Epilepsia. 2015; 56(10): 1515-23.
- Gaínza-Lein M, Fernández IS, Ulate-Campos A, Loddenkemper T, Ostendorf Timing in the treatment of status epilepticus: from basics to the clinic. Seizure. 2019; 68: 22-30.
- Arya R, Kothari H, Zhang Z, Han B, Horn PS, Glauser TA. Efficacy of nonvenous medications for acute convulsive seizures: A network meta analysis. Neurology 2015; 85 (21):1859-68.
- Glauser T, Shinnar S, Gloss D, Alldredge B, Arya R, Bainbridge J, et Evidence-based guideline: treatment of convulsive status epilepticus in children and adults: report of the Guideline Committee of the American Epilepsy Society. Epilepsy Curr. 2016; 16(1): 48-61.
- Alvarez V, Lee JW, Drislane FW, Westover MB, Novy J, Dworetzky BA, et al. Practice variability and efficacy of clonazepam, lorazepam, and midazolam in status epilepticus: a multicenter Epilepsia. 2015; 56(8): 1275-85.
- Chamberlain JM, Okada P, Holsti M, Mahajan P, Brown KM, Vance C, et Lorazepam vs diazepam for pediatric status epilepticus: a randomized clinical trial. JAMA. 311(16): 1652-60.
- Bleck T, Cock H, Chamberlain J, Cloyd J, Connor J, Elm J, et al. The established status epilepticus trial Epilepsia. 2013; 54 (Suppl 6): 89-92.
- Glauser T, Shinar S, Gloss D, Alldredge B, Arya R, Bainbridge J, et Evidence based guideline: treatment of convulsive status epilepticus in children and adults. Report of the guideline committee of the American Epilepsy Society. Epilepsy Current. 2016; 16(1): 48-61.
- Husain AM, Lee JW, Kolls BJ, Hirsch LJ, Halford JJ, Gupta PK, et al. Critical Care EEG Monitoring Research Consortium. Randomized trial of lacosamide versus fosphenytoin for nonconvulsive Ann Neurol. 2018; 83(6): 1174-85.
- Fujikawa Starting ketamine for neuroprotection earlier than its current use as an anesthetic/antiepileptic drug late in refractory status epilepticus. Epilepsia. 2019; 60(3): 373-80.
- Toledano R, Gil-Nagel A. Adverse effects of antiepileptic drugs. Semin Neurol. 2008; 28(03): 317-27.

