INTRODUCCIÓN. ELECTROENCEFALOGRAMA Y REQUISITOS TÉCNICOS
El electroencefalograma (EEG) es el método diagnóstico que permite la evaluación de los potenciales eléctricos generados por la actividad cerebral, siendo registrados por medio de electrodos situados bien sobre la superficie del cuero cabelludo (electrodos no invasivos) o a nivel cerebral profundo (invasivos), siendo una prueba repetible, accesible y económica. Es el método diagnóstico más útil para el estudio de la epilepsia y el más específico para estudiar el córtex epileptogénico. Sin embargo, es un test que tiene sus limitaciones siendo importante conocer que un EEG normal no excluye epilepsia, ya que el 10 % de epilépticos no muestran anomalías. Esto se debe a que existe una parte importante del córtex cerebral que no es accesible a electrodos de superficie (estructuras mesiales, basales, ínsula y corteza orbitofrontal) y a que gran parte de las descargas epileptiformes intercríticas (DEI) no son registradas si afectan a un área menor de 10 cm2 de corteza cerebral. Por otro lado, la presencia de actividad epileptiforme puede darse en diferentes contextos clínicos no implicando, por sí misma, el desarrollo de crisis epilépticas.
La Federación Internacional de Sociedades de Electroencefalografía y Neurofisiología Clínica (1958) desarrolló el sistema Internacional 10-20, permitiendo una unificación en la terminología y localización de los electrodos. Su posición es determinada utilizando cuatro puntos de referencia de estructuras anatómicas del cráneo (nasión, inion y puntos preauriculares) y las distancias entre electrodos se miden en porcentajes y no en valores absolutos, de tal modo que los electrodos están separados un 10 % o un 20 % de la distancia total entre un par de puntos de referencias craneales. El sistema 10-10, propuesto años después, incluye electrodos adicionales en posiciones intermedias al sistema 10-20 y permite realizar registros con mayor densidad de electrodos, a fin de lograr una mejor localización de las DEI en determinados casos o realizar estudios orientados a cirugía de la epilepsia30 (fig. 2).
El sistema 10-20 se recomienda a partir de los 5 años de edad. A edades más tempranas es preferible utilizar menor número de electrodos, dada la dificultad para su ubicación por el tamaño de la cabeza. Un mayor número de electrodos en niños pequeños no aumenta la posibilidad de detectar anomalías focales. Sin embargo, puede ser necesaria la colocación de electrodos adicionales en el estudio de de-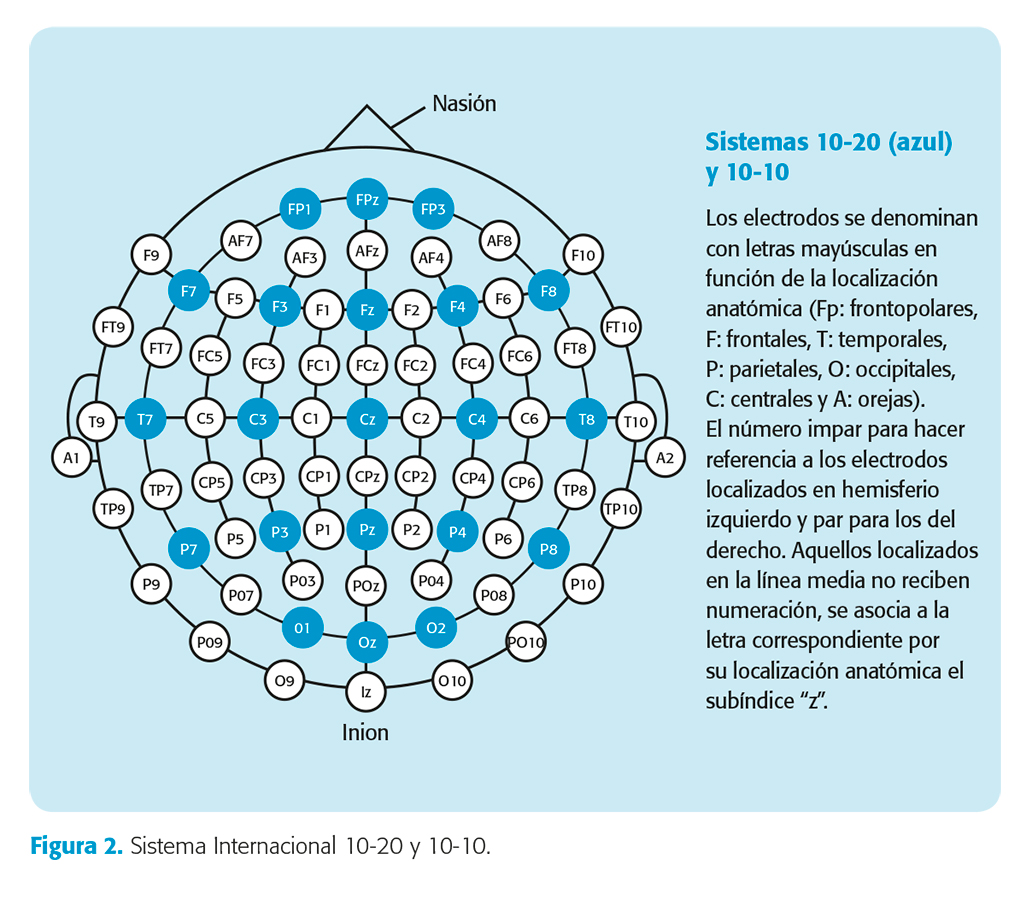 terminadas epilepsias con posible foco epileptógeno más profundo, sobre todo de origen temporal.
terminadas epilepsias con posible foco epileptógeno más profundo, sobre todo de origen temporal.
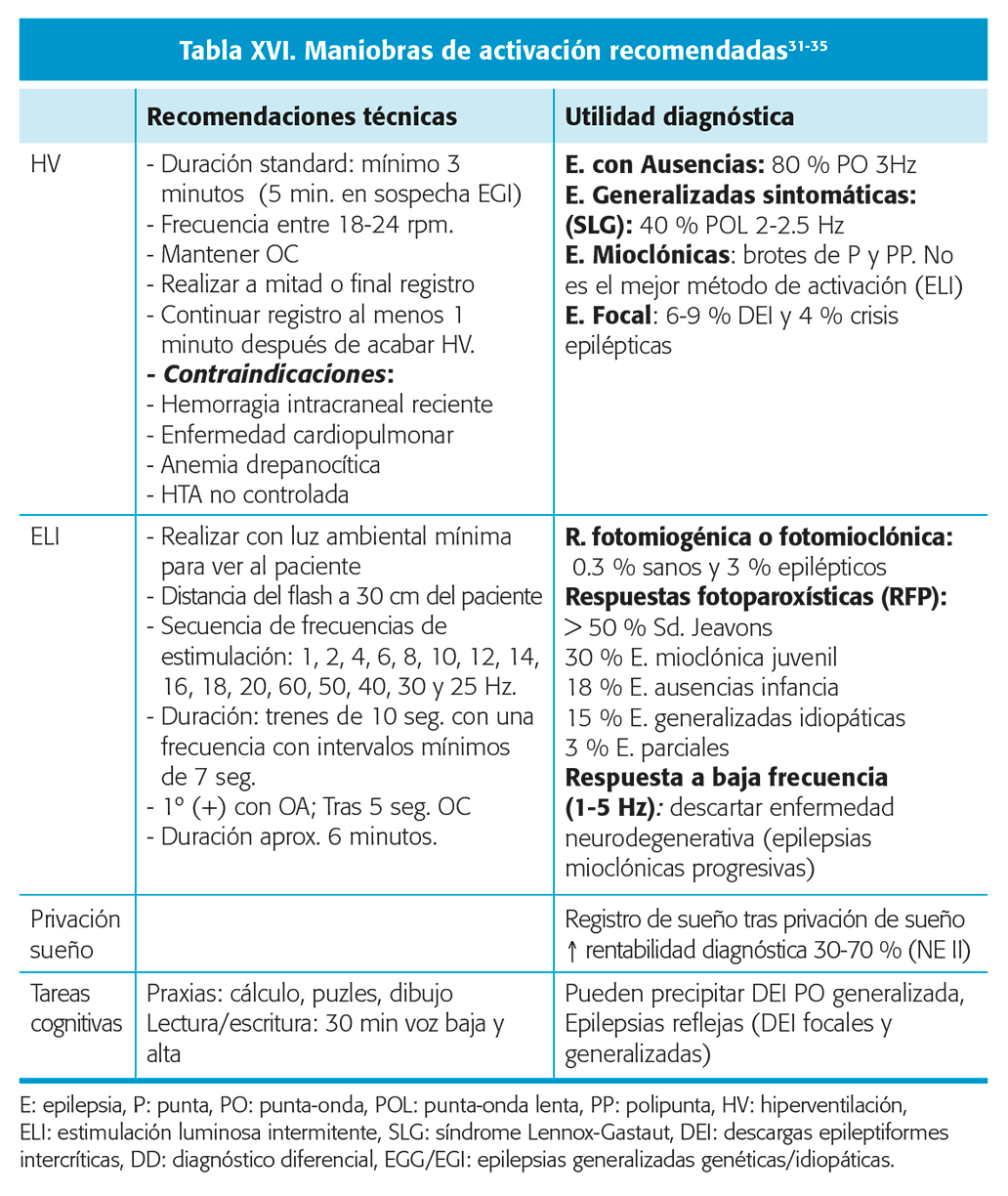
Todo EEG debe satisfacer unos requisitos técnicos y si la situación clínica lo permite, incorporar maniobras de activación (tablas XV y XVI).
Las técnicas de activación habituales en la práctica clínica habitual (hiperventilación, ELI, privación de sueño y sueño) aumentan la excitabilidad cortical. Nivel de evidencia I. En casos de EGG/EGI las técnicas de activación específicas (HV y ELI) son superiores a la reiteración de EEG basales para la detección de DEI. Nivel de evidencia III. La realización de un EEG al despertar tras siesta breve en conjunción con hiperventilación y ELI puede incrementar la sensibilidad para registrar DEI hasta el 90 % de los pacientes con EGG/EGI. Nivel de evidencia I32.
Las técnicas de sugestión se utilizan en casos de sospecha de trastornos paroxísticos no epilépticos o crisis psicógenas, pero pueden conllevar falsos positivos en algunos casos. Nivel de evidencia III.

INDICACIONES DEL ELECTROENCEFALOGRAMA EN LA EPILEPSIA34,38,39
- Establecer riesgo de recurrencia tras una primera crisis y confirmar diagnóstico de epilepsia en algunas situaciones.
- Clasificación del tipo de epilepsia y síndromes epilépticos dentro del contexto clínico.
- Tipificación de los eventos paroxísticos y diagnóstico diferencial con crisis epilépticas.
- Cuantificación de algunos tipos de crisis.
- Respuesta al tratamiento en algunos síndromes epilépticos.
- Pronóstico tras cirugía de la epilepsia.
- Estatus epiléptico (EE): diagnóstico de EE no convulsivo (EENC) y monitorización de la respuesta al tratamiento del EE.
- Otras indicaciones, más allá del estudio de la epilepsia son la valoración del daño cerebral en paciente neurocrítico, maduración cerebral en prematuros y diagnóstico de muerte encefálica.
EEG EN LA CLASIFICACIÓN DEL TIPO DE CRISIS Y SÍNDROMES EPILÉPTICOS
Rara vez, el EEG de un individuo asintomático muestra DEI y en ese caso, la posibilidad de desarrollar una epilepsia es entre 2-3 %. Nivel de evidencia IV. El diagnóstico de epilepsia se basa en la clínica y la presencia de descargas epilépticas interictales (DEI), en un adecuado contexto clínico, confirma el diagnóstico de epilepsia, así como también la detección de DEI en EEG basales sugiere mayor riesgo de recurrencia de una crisis epiléptica. Nivel de evidencia I. En los casos en los que no exista una confirmación de epilepsia, ya sea por falta/inconsistencia de los datos clínico o bien por no detectarse DEI en los estudios EEG convencionales, se requiere de estudios EEG prolongados, siendo el registro ictal de las crisis el patrón oro diagnóstico.
Las DEI más comunes son las puntas, ondas agudas y los complejos punta-onda, pudiendo ser focales o generalizados (fig. 3). Los registros realizados en el transcurso de las primeras 24 horas después de una crisis aumentan la probabilidad de detectar DEI (Nivel de evidencia II) y el consumo de FAE disminuye la probabilidad de detectar DEI. Nivel de evidencia IV.
Existen una serie de patrones EEG característicos de algunos tipos de epilepsia focales y generalizadas (tabla XVII). El rasgo distintivo de las epilepsias generalizadas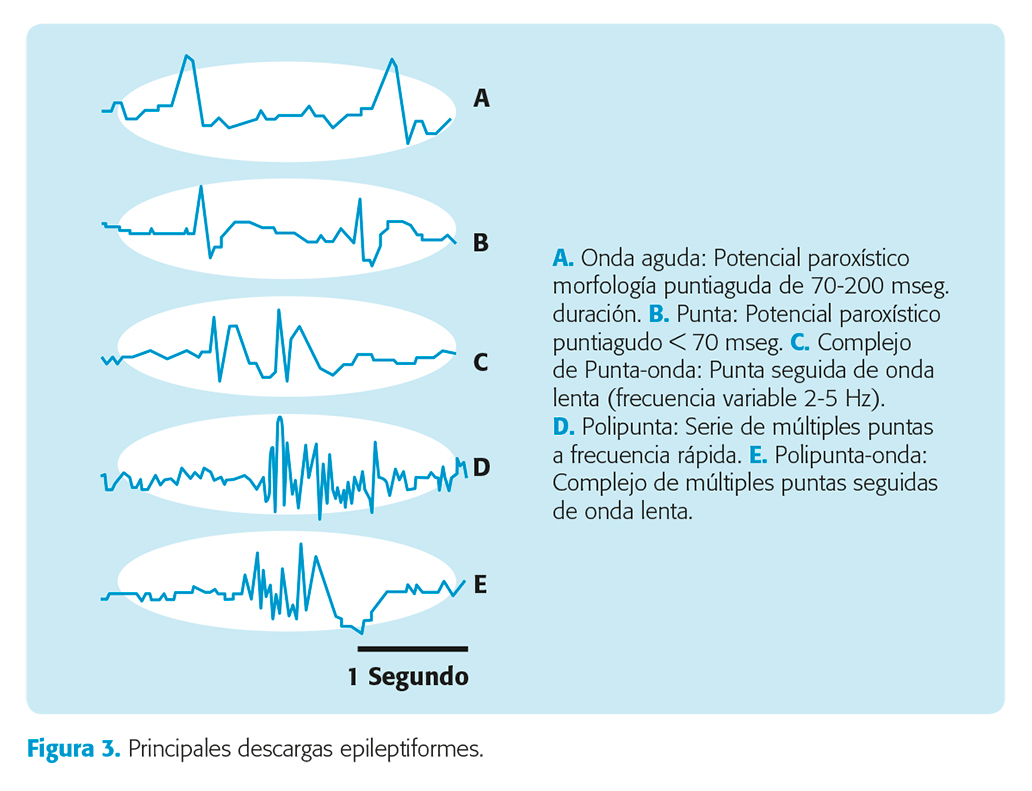 es el complejo de punta-onda generalizada con un máximo anterior. Frecuencias de 3-5 Hz sobre una actividad de fondo normal son características de EGG/EGI, mientras que la punta-onda lenta < 2,5Hz sobre una actividad de fondo lenta, aparece en epilepsias sintomáticas y encefalopatías epilépticas. La morfología de las DE es similar en patrones ictales e interictales, sugiriendo una duración < 3 segundos para las descargas ictales. Nivel de evidencia III33,38. En cuanto a las epilepsias focales del adulto, las DEI son más frecuentes en epilepsias temporales que en las epilepsias extratemporales. Nivel de evidencia IV. DEI en región temporal anterior, así como actividad temporal delta rítmica intermitente se correlacionan con epilepsia temporal medial. Nivel de evidencia II. La actividad focal theta rítmica es el patrón ictal más frecuente en esclerosis mesial temporal y predice libertad de crisis tras cirugía32,33. Nivel de evidencia I. En las epilepsias extratemporales las DEI registradas en EEG de superficie tienden a tener menor valor localizador dada su tendencia a la lateralización, propagación a regiones distantes y sincronía bilateral secundaria. Los patrones ictales se registran con menor frecuencia que en epilepsias temporales y tiene escaso valor localizador32.
es el complejo de punta-onda generalizada con un máximo anterior. Frecuencias de 3-5 Hz sobre una actividad de fondo normal son características de EGG/EGI, mientras que la punta-onda lenta < 2,5Hz sobre una actividad de fondo lenta, aparece en epilepsias sintomáticas y encefalopatías epilépticas. La morfología de las DE es similar en patrones ictales e interictales, sugiriendo una duración < 3 segundos para las descargas ictales. Nivel de evidencia III33,38. En cuanto a las epilepsias focales del adulto, las DEI son más frecuentes en epilepsias temporales que en las epilepsias extratemporales. Nivel de evidencia IV. DEI en región temporal anterior, así como actividad temporal delta rítmica intermitente se correlacionan con epilepsia temporal medial. Nivel de evidencia II. La actividad focal theta rítmica es el patrón ictal más frecuente en esclerosis mesial temporal y predice libertad de crisis tras cirugía32,33. Nivel de evidencia I. En las epilepsias extratemporales las DEI registradas en EEG de superficie tienden a tener menor valor localizador dada su tendencia a la lateralización, propagación a regiones distantes y sincronía bilateral secundaria. Los patrones ictales se registran con menor frecuencia que en epilepsias temporales y tiene escaso valor localizador32.
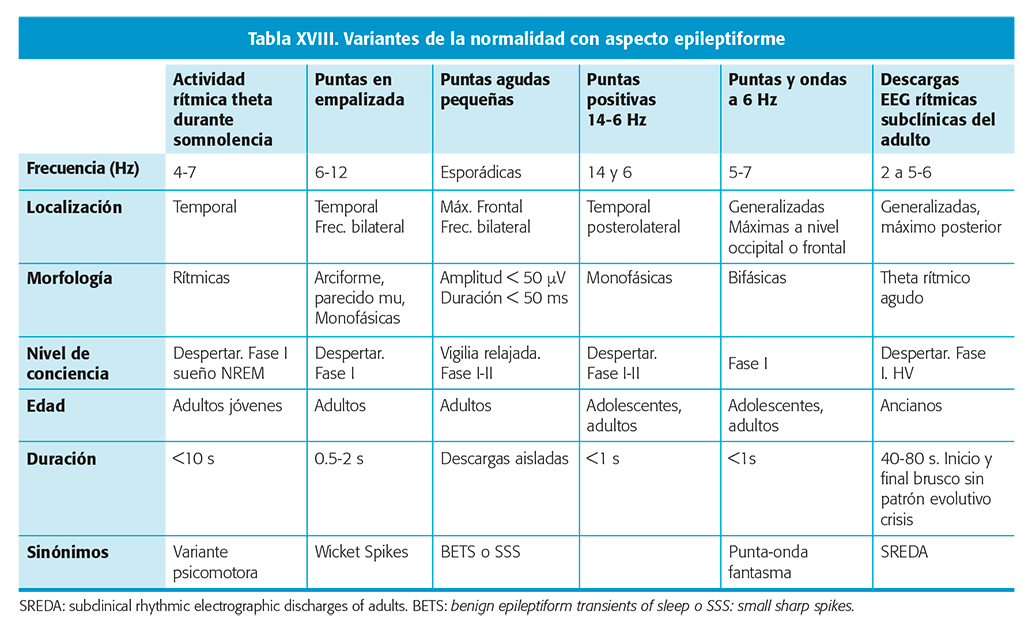
Existen variantes agudas fisiológicas en el EEG (tabla XVIII) que deben diferenciarse de patrones epileptiformes ictales o interictales para evitar la interpretación errónea del registro EEG y la conclusión equívoca de diagnóstico de epilepsia.

TIPOS DE ESTUDIOS ELECTROENCEFALOGRÁFICOS
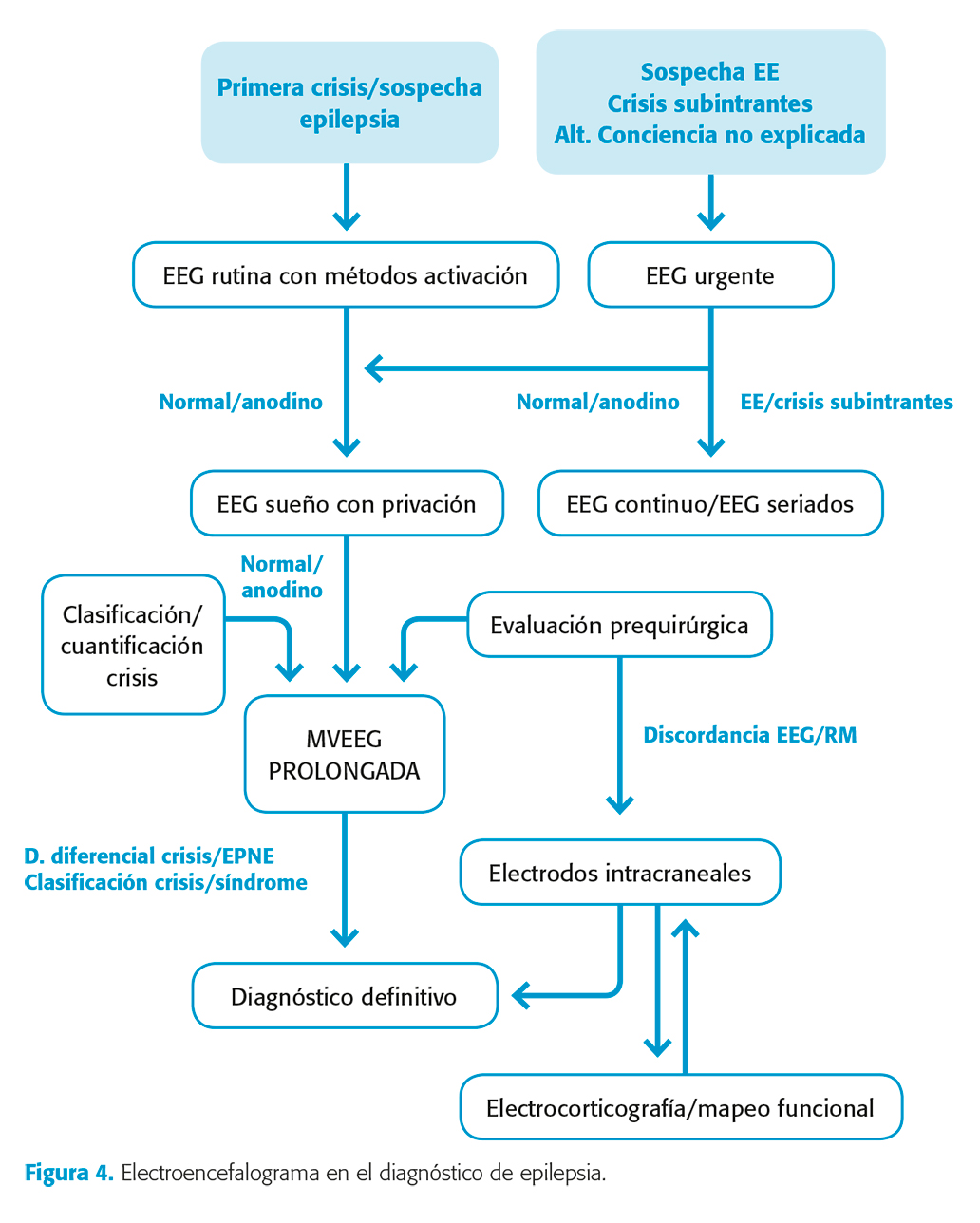
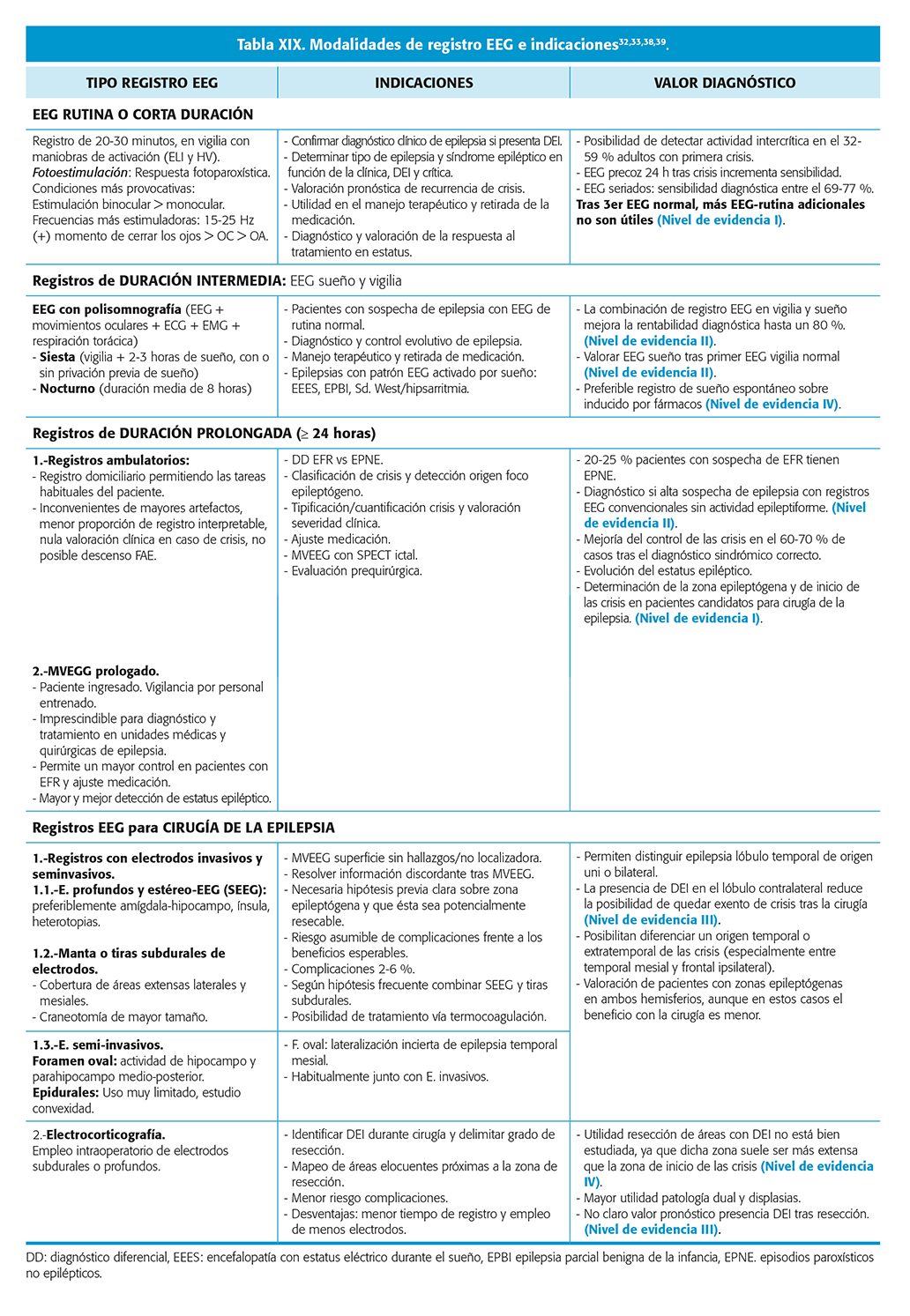
Dependiendo del tipo de crisis y epilepsia, congruencia de los hallazgos clínicos y neurofisiológicos con las pruebas de neuroimagen, así como la evolución y respuesta al tratamiento, será necesario estratificar los estudios electroencefalográficos que debemos realizar, tanto con fines diagnósticos como terapéuticos (fig. 4 y tabla XIX).
EEG Y TRATAMIENTO ANTIEPILÉPTICO
El rol del EEG en el seguimiento del tratamiento es incierto. Disponemos de resultados contradictorios en estudios sobre epilepsias focales. En EGG/EGI, fármacos como el ácido valproico o las benzodiacepinas suprimen de manera clara las DEI y la respuesta fotoparoxística, lo que se ha correlacionado con el control de las crisis de ausencias y otros tipos de crisis generalizadas38.
Existe una clara correlación entre el control clínico y la desaparición de las DEI en las ausencias típicas. Nivel de evidencia II. Para otro tipo de epilepsias esta relación no es tan evidente38.
En pacientes con epilepsia controlada con FAE, libres de crisis durante 4-5 años, existe un elevado riesgo de recurrencia si se registran DEI en los EEG previos a retirada. Nivel de evidencia II. La probabilidad de encontrar DEI es mayor en estudios más prolongados. Nivel de evidencia III. Este riesgo se ve también condicionado por el tipo de síndrome epiléptico y la duración del registro EEG que se realice previo a la retirada farmacológica32.
EEG COMO MARCADOR PRONÓSTICO TRAS CIRUGÍA DE LA EPILEPSIA
La ausencia de DEI en el EEG de superficie a los 6-12 meses de cirugía se asocia con buen resultado38. Entre 1-3 meses el valor del EEG tiene escasa significación, tampoco parece concluyente la presencia de DEI en la electrocorticografía post-reseccion38.
EEG URGENTE
La realización de un EEG lo más precozmente posible tras una crisis, detecta mayor frecuencia de DEI que un registro demorado más de 24-48 h. Nivel de evidencia I. En el caso de una primera crisis tiene valor pronóstico y puede establecer el diagnóstico de epilepsia y la necesidad de tratamiento con FAE, por lo que debe ser considerado si se dispone de la técnica.
En el estatus epiléptico
Debe realizarse un EEG urgente a todo paciente con sospecha de EENC, con alteración del nivel de conciencia no explicada por otras causas o no recuperación tras el tratamiento de un EE convulsivo. El EEG es esencial para el correcto diagnóstico y manejo del EE, y resulta criterio indispensable para el diagnóstico de EENC. El EENC es una entidad muy heterogénea desde el punto de vista clínico y hasta la fecha no disponemos de criterios diagnósticos electroencefalográficos basados en la eviden- cia (tabla XX)40. La demora en su diagnóstico y tratamiento es un factor pronóstico negativo independiente de la causa.
cia (tabla XX)40. La demora en su diagnóstico y tratamiento es un factor pronóstico negativo independiente de la causa.
Hoy en día se recomienda la realización de EEG continuo (EEGc) o MVEEG para una mejor evaluación de tipo de estatus epiléptico, su duración y respuesta al tratamiento.
En el paciente crítico
Se registran crisis electrográficas entre el 19-27 % de pacientes adultos con patología aguda grave, la mayoría en las primeras 24 horas. Nivel de evidencia II. Hasta el 16 % de pacientes de UCI quirúrgica presentan crisis no convulsivas y un 48 % de pacientes persisten en ENC tras tratamiento del EE convulsivo32. Por tanto, el EEG continuo (EEGC) tiene un papel importante en la detección de crisis y ENC en el paciente crítico32,42 (tabla XXI). Su duración mínima recomendada es de 24 horas (Nivel de evidencia II) y su interpretación, debe ser lo más precoz posible dependiendo del contexto clínico, interviniendo técnicos con diferentes niveles de especialización, siendo preciso la revisión por un electroencefalografista al menos dos veces al día. Nivel de evidencia IV. Es altamente recomendable que el EEGC se realice con registro simultáneo con vídeo. La presencia de patrones EEG de significado incierto como la actividad periódica generalizada, bilateral o lateral y la actividad delta rítmica focal, se asocian con mayor frecuencia a EENC tanto en adultos como en niños y deberá ser considerada motivo de la realización de EEGC o en su defecto estudios EEG seriados en el contexto clínico adecuado42

Bibliografía
- American clinical neurophysiology Society. Guideline 2: Guidelines for standard electrode position J Clin Neurophysiol. 2016; 33: 308-11.
- American clinical neurophysiology Guideline1: Minimum technical requirements for performing clinical electroencephalography. J Clin Neurophysiol 2016; 33: 300-8.
- Tatum WO, Rubboli G, Kaplan PW, Mirsatari SM, Radhakrishnan K, Gloss D, et al. Clinical utility of EEG in diagnosing and monitoring epilepsy in adults. Clinical Neuro 2018; 129: 1056-82.
- Koutroumanidis M, Arzimanoglou A, Caraballo R, Goyal S, Kaminska A, Laoprasert P, et The role of EEG in the diagnosis and classification of the epilepsy syndromes: a tool for clinical practice by the ILAE Neurophysiology Task force (part 1). Epileptic disord. 2017; 19: 233-98.
- Koutroumanidis M, Arzimanoglou A, Caraballo R, Goyal S, Kaminska A, Laoprasert P, et The role of EEG in the diagnosis and classification of the epilepsy syndromes: a tool for clinical practice by the ILAE Neurophysiology Task force (part 2). Epileptic disord. 2017;19: 385-437.
- Giorgi FS, Guida M, Caciagli L, Maestri M, Carnicelli L, Bonnani E, et What is the role for EEG after sleep deprivation in the diagnosis of epilepsy? Issues, controversies and future directions. Neurosci Biobehav Rev. 2014; 47: 533-48.
- Sánchez JC, Ruiz J, Roldán S, Serrano P. Guía andaluza de Epilepsia 2015. Barcelona: Viguera Ed;
- Blanco T, Rubio Indicaciones del electroencefalograma en Epilepsia. En: Villanueva V. and Sancho J. Guía práctica de Epilepsia de la Comunidad Valenciana 2010 p17-30. Disponible en ww2.castellon.san.gva.es.
- Rosenow F, Martin K, Hamer HM. Non-invasive EEG evaluation in epilepsy diagnosis. Expert Rev 2015; 15: 425-44.
- Jayakar P, Gotman J, Harvey AS, Palmini A, Tassi L, Schomer D, et Diagnostic utility of invasive EEG for epilepsy surgery: indications, modalities, and techniques. Epilepsia. 2016; 57: 1735-47.
- Beniczky S, Hirsch LJ, Kaplan PW, Pressler R, Bauer G, Aurlien H, et Unified EEG terminology and criteria for nonconvulsive status epilepticus. Epilepsia. 2013; 54 (suppl6): 28-9.
- Leitinger M Beniczky S, Rohracher A, Gardella E, Kalss G, Qerama E, et Salzburg consensus criteria for non-convulsive status epilepticus. Epilepsy Behav. 2015; 49: 158-163.
- Herman ST, Abend NS, Bleck TP, Chapman KE, Drislane FW, Emerson RG, et al. Consensus statement on continuous EEG in critically ill adults and children, part I: J Clin Neurophysiol. 2015; 32: 87-95.

